BENTO Trial
Informationen für zuweisende Ärzte
und interessierte Studienzentren

Gemeinsam Forschung vorantreiben:
Ihre Rolle in unserer laufenden Studie
Herzlich willkommen!
Unser Ziel ist es, gemeinsam neue Erkenntnisse zu gewinnen und die Patientenversorgung zu verbessern.
Hier finden Sie die wichtigsten Informationen zur Erprobungsstudie BENTO als zuweisender Facharzt oder als interessiertes Studienzentrum.
Bronchoskopische Vaportherapie (BTVA)
Bei der Thermoablation, auch als bronchoskopische Vaportherapie (BTVA) bezeichnet, wird heißer Wasserdampf zielgerichtet in das geschädigte Lungengewebe eingebracht. Dies führt zu einer lokalen Entzündungsreaktion und im weiteren Verlauf zu einer Schrumpfung des funktionslosen überblähten Lungengewebes. Dadurch soll bewirkt werden, dass den noch funktionsfähigen Lungenanteilen mehr Raum zur Verfügung steht.
Diese Erprobungsstudie untersucht, ob Patienten mit schwerem Lungenemphysem von einer bronchoskopischen Lungenvolumenreduktion mittels Bronchoscopic Thermal Vapor Ablation (BTVA) profitieren.
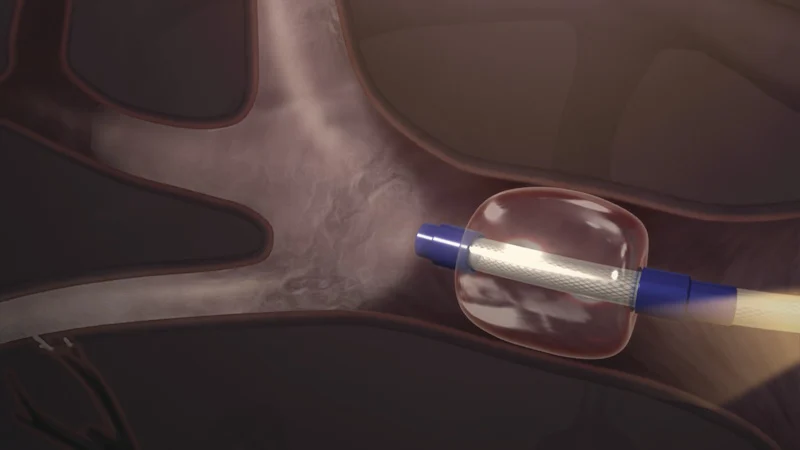
Quelle: Uptake Medical Technology
Studienziel und Design
- BENTO ist eine Studie im Auftrag des Gemeinsamen Bundesausschusses (G-BA) zur Erprobung der bronchoskopischen Lungenvolumenreduktion mittels Thermoablation beim schweren Lungenemphysem
- BENTO wird von der IHF GmbH Institut für Herzinfarktforschung in Zusammenarbeit mit dem Studienleiter Herr Prof. Dr. med. Felix Herth (Thoraxklinik Heidelberg) durchgeführt und wissenschaftlich begleitet
- BENTO ist eine prospektive, 2-armige, randomisierte (2:1), multizentrische, offene sonstige klinische Prüfung gemäß Artikel 82 der Verordnung (EU) 2017/745 (MDR)
Rationale
Die Erprobungsstudie soll dazu beitragen, den Nutzen dieses Verfahrens als eine wirksame und sichere Behandlungsoption zu belegen, um Emphysempatienten eine ausreichende, zweckmäßige und wirtschaftliche Versorgung unter Berücksichtigung evidenzbasierter medizinischer Erkenntnisse zu gewährleisten.
Ein positives Ergebnis dieser Erprobungsstudie wird den Weg in eine Kostenerstattung dieser Behandlung durch die gesetzlichen Krankenkassen öffnen.
Informationen für zuweisende Ärzte
Ihre Rolle als zuweisender Arzt:
- Identifikation möglicher Patienten – unterstützen Sie uns, indem Sie mögliche Patienten identifizieren, die potentiell für die Studie infrage kommen könnten
- Erstkontakt: Stellen Sie den Kontakt zwischen Ihrem Patienten und Studienteam her*.
- Überweisung ins Krankenhaus und Fachambulanzen Ihrer Patienten zur weiteren Behandlung
Vorteile für Ihre Patienten:
- Zugang zu innovativen Therapien: Teilnahme an einer weiteren Behandlungsmöglichkeit, die außerhalb der Studie für KK-Patienten noch nicht verfügbar ist.
- Individuelle Betreuung Ihrer Patienten durch Expertenteams am Studienzentrum
Hinweise:
Die Untersuchung Ihres Patienten und Feststellung der Eignung für eine mögliche Teilnahme erfolgt durch das Studienteam am Studienzentrum.
In die Studie können nur gesetzlich krankenversicherte Patienten aufgenommen werden. Bitte kontaktieren Sie im Falle eines Privatpatienten dennoch das Studienzentrum, damit Ihrem Patienten geholfen werden kann.
Informationen für interessierte Studienzentren
Voraussetzungen für Studienzentren
- Ihr Haus verfügt über eine Fachabteilung für Pneumologie oder Innere Medizin mit Schwerpunkt Pneumologie und vorgegebene strukturelle Anforderungen
- Erfahrung mit der bronchoskopischen Lungenvolumenreduktion (BTVA) mittels Thermoablation
- Bereitschaft zum Einsatz des InterVapor®-Systems nach einem individuellen Behandlungsplan
- Das Studienteam (Ärzte, Schwestern) hat Erfahrung in klinischen Studien mit Medizinprodukten
- Zugang zur geeigneten Patientengruppe
- Einhaltung regulatorischer Standards (MDR und ISO14155)
- Möglichkeit zur ambulanten Nachsorge
Vorteile für Ihr Studienzentrum und einer Zusammenarbeit
- Verbesserung der Patientenversorgung
- Beitrag zur innovativen Forschung
- Etablierung und Anwendung einer neuen, innovativen Behandlungsmethode des Lungenemphysems
Kontaktieren Sie uns für weitere Informationen
Interessiert?
→ Für zuweisende Ärzte:
Prof. Felix Herth
E-mail: felix.herth@med.uni-heidelberg.de
Telefon: +49 6221 396 1200
→ Für interessierte Studienzentren:
Bitte kontaktieren Sie unsere Studienleitung für weitere Informationen:
Nancy Hofmann
E-mail: Nancy.Hofmann@ihf.de
Telefon: +49 621 595 77 214
Leschek Brachmann
E-mail: Leschek.Brachmann@ihf.de
Telefon: +49 621 595 77 225
Let's get talking!
Would you like to learn more, start your project or have another request?
Patientengruppe und Ein- und Ausschlusskriterien
Falls Sie ganz genau wissen möchten, um welche Patienten es in der Studie geht, finden Sie hier alle Ein- und Ausschlusskriterien!
Hinweis:
Die im Folgenden aufgeführten Kriterien für eine Aufnahme in die klinische Prüfung sollen Ihnen lediglich einen Überblick zur gesuchten Patientenpopulation geben. Als zuweisender Arzt müssen sie diese Kriterien im Einzelfall nicht verifizieren. Bitte nehmen Sie gerne vorab Kontakt mit einem für Sie in Frage kommenden, teilnehmenden Studienzentrum auf (Verlinkung auf die GBA Seite mit den Zentren).
Eine genaue Untersuchung des Patienten und Verifizierung aller Ein- und Ausschlusskriterien wird am teilnehmenden Studienzentrum durchgeführt. Letztlich entscheidet eine interdisziplinäre Fallkonferenz bestehend aus Ärzten der Fachrichtungen Pneumologie, Radiologie und Thoraxchirurgie über die Behandlung eines Patienten / einer Patientin gemäß §3 der Richtlinie über Maßnahmen zur Qualitätssicherung nach § 136 Absatz 1 Satz 1 Nummer 2 SGB V für die stationäre Versorgung mit Verfahren der bronchoskopischen Lungenvolumenreduktion beim schweren Lungenemphysem (QS-RL BLVR)
Einschlusskriterien
- Alter: ≥ 40 Jahre und ≤ 75 Jahre
- vom Patienten erhaltene schriftliche Einwilligung nach erfolgter Aufklärung
- schweres Lungenemphysem mit Indikation zur BTVA (Bronchoscopic Thermal Vapor Ablation):
- bilaterales heterogenes Emphysem der Oberlappen im GOLD-Stadium 3-4 und
- Nachweis des schweren Lungenemphysems in der hochauflösenden Computertomographie (nicht älter als 6 Monate vor Einschluss) und
- funktioneller Nachweis einer schweren Lungenüberblähung und
- FEV1 post Lyse zwischen 20% und < 45% (kalkuliert) und
- Totalkapazität (TLC) ≥ 100% (kalkuliert) und
- Residualvolumen (RV) > 175% (kalkuliert) und
- arterielle Blutgaswerte von: PaCO2 ≤ 50 mmHg; PaO2 > 50 mmHg bei Raumluft und
- ausgeprägte Dyspnoe mit einem Wert ≥ 2 auf der modifizierten Skala des Medical Research Council (mMRC) und
- 6-Minuten-Gehtest > 140 Meter
- patientenindividuelle, präinterventionelle Ausschöpfung der konservativen Behandlungsmöglichkeiten:
- optimierte medizinische Therapie (gemäß den GOLD-Richtlinien) und
- Nichtraucher seit 6 Monaten vor Einschluss
- Nachweis einer abgeschlossenen pulmonalen oder geriatrischen Rehabilitation in den letzten 4 Jahren
- ≥ 6 Wochen ambulant oder
- ≥ 3 Wochen stationär oder
- Alleinige Teilnahme an regelmäßigen körperlichen Aktivitäten, die über die Aktivitäten des täglichen Lebens hinausgehen (z.B. ein Gehprogramm)
- Nach Einschätzung des Prüfarztes mental und körperlich in der Lage, an den Studienprozeduren und -visiten mitzuwirken
- Indikationsstellung im Rahmen einer interdisziplinären Fallkonferenz mit Fachärzten für Pneumologie, Radiologie und Thoraxchirurgie gemäß §3 der Richtlinie über Maßnahmen zur Qualitätssicherung nach § 136 Absatz 1 Satz 1 Nummer 2 SGB V für die stationäre Versorgung mit Verfahren der bronchoskopischen Lungenvolumenreduktion beim schweren Lungenemphysem (QS-RL BLVR)
Ausschlusskriterien
- jeder Zustand, der die Durchführung der Nachuntersuchungen der klinischen Prüfung oder der Bronchoskopie behindern oder das Ergebnis der klinischen Prüfung beeinträchtigen würde
- DLCO* < 20% (kalkuliert)
- Body-Mass-Index (BMI) < 18 kg/m2 oder > 32 kg/m2
- pulmonale Hypertonie
- systolischer PAP-Spitzenwert > 45 mmHg oder mittlerer PAP >25 mmHg
- PAP -Wert: Rechtsherzkatheter-Messungen werden gegenüber Echokardiogramm-Messungen als maßgebend angesehen
- klinisch signifikante Bronchiektasen
- Pneumothorax oder Pleuraergüsse innerhalb der letzten 6 Monate
- Herz- und/oder Lungentransplantation, chirurgische Lungenvolumenreduktion (LVRS), Bullektomie, Lobektomie oder Pneumonektomie, Pleurodese oder jegliche Operation in den Targetlappen (Oberlappen)
- kürzliche Atemwegsinfektionen oder COPD-Exazerbation in den letzten 6 Wochen
- instabile COPD:
- COPD-bedingte Krankhausaufenthalte, die Antibiotika erforderten, in den letzten 12 Monaten
- COPD-bedingter Krankenhausaufenthalt in den letzten 3 Monaten
- tgl. Einnahme von systematischen Steroiden, >5mg Prednisolon
- einzelne große Bulla (definiert als > 1/3 des Volumens des Lappens) im Oberlappen oder eine paraseptale Emphysemverteilung im zu behandelten Lappen
- Koagulopathie oder derzeitige Einnahme von Antikoagulantien, die nicht pausiert werden können (außer ASS ≤ 100mg/ pro Tag)
- Patienten mit gegenwärtigen endobronchialen Ventilen oder mit vor weniger als 6 Monaten explantierten Ventilen im Ziellappen in einem mit InterVapor® zu behandelnden Segment
- Patienten mit implantierten, endobronchialen Spiralen (Coils)
- Patienten mit vorheriger endobronchialer Polymer-/ Klebstoff-Behandlung
- Patienten mit Immunsystemstörungen oder Begleiterkrankungen, die die Einnahme von Immunsuppressiva von klinischer Relevanz notwendig machen
- Vorgeschichte einer der folgenden Bedingungen:
- Myokardinfarkt oder akutes Koronarsyndrom im vorangegangenen Jahr
- Krankenhausaufenthalt wegen Linksherzversagen im letzten Jahr
- klinisch führende Asthmaerkrankung oder Alpha-1-Antitrypsin-Mangel
- bekannte Empfindlichkeit gegenüber Medikamenten, die zur Durchführung einer Bronchoskopie erforderlich sind
- Lebenserwartung <12 Monate
- neu verschriebene Morphinderivate innerhalb der letzten 4 Wochen
- Schwangerschaft zum Zeitpunkt des Einschlusses
